


 |
 |
 |
Les plaquettes sont des élément anucléés, leur analyse se rapproche en plusieurs points de celle des érythrocytes.
2. Les dysfonctionnements plaquettaires.
La durée de vie des plaquettes est limitée à une période de 3 à 10 jours. Les thrombocytopénies centrales sont donc rapidement observables sur l'hémogramme.
Chien |
Chat |
|
| Normes | >200000 |
>300000 |
| Risque de saignements | <30000 |
<30000 |
| Seuil de transfusion | <3000 |
<3000 |
Le nombre de plaquettes circulantes n'est pas toujours très significatif, la masse plaquettaire est le réel indicateur. Cette masse dépend :
Etant donné la difficulté d'obtenir une évaluation fiable de cette masse plaquettaire, on s'aidera du temps de saignement et de la clinique :
Le myélogramme est souvent nécessaire pour distinguer les thrombocytopénies centrales des thrombocytopénies périphériques. En effet la mise en évidence des plaquettes réticulées (contenant beucoup d'ARN), nécessite un examen en cytométrie de flux, après coloration au thiazole orange, ce qui est rarement disponible en routine. La mesure du volume plaquettaire moyen et la mise en évidence de grandes plaquettes permettent parfois de suspecter une régénération plaquettaire active. La fiabilité de ces paramètres n'est cependant pas constante. Enfin les thrombocytopénies mixtes sont relativement fréquentes.
Il existe trois grandes causes de thrombocytopénies périphériques : la destruction, la consommation excessive et la ségrégation. Bien souvent la cause de la thrombocytopénie n'est pas déterminée, elle peut même mettre en jeu les trois mécanismes combinés.
1.1.1. Thrombocytopénies immunes.
Comme les Anémie Hémolytiques Immunes (AHI) elles sont dites primaires ou secondaires. Dans les deux cas elles sont souvent associées à une AHI et dans ce cas on parle de syndrome d'Evans.
L'étiologie immunitaire nécessite un dosage des immunoglobulines adhérentes à la surface des plaquettes (PSAIg). Ce test doit être fait au chevet du malade et n'est que très rarement mis en oeuvre en pratique. Ce test ne permet pas de différencier les formes primaires des formes secondaires.
1.1.1.1. Les thrombocytopénies immunes primaires.
Elles font intervenir des anticorps anti-plaquettes (souvent anti-GPIIIa ou GPIIIb) qui ne sont pas induits par une autre pathologie. Ces anticorps sont aussi fréquemment dirigés contre les mégacaryoblastes, ce qui produit des trombocytopénies sévères périphériques et centrales.
Les femelles et les Cockers spaniel semblent prédisposés.
1.1.1.2. Les thrombocytopénies immunes secondaires.
Elles font intervenir des anticorps dirigés contre des antigènes (virus, bactéries, médicaments, tumeurs) adsorbés à la surface des plaquettes ou des immuns-complexes interagissant avec les plaquettes. On les rencontre essentiellement lors de :
Plus rarement, elles se rencontrent lors de :
Des formes iatrogènes existent, mais leur mécanisme n'est pas toujours bien connu :
Elles sont souvent de mauvais pronostic.
Les éléments objectifs essentiels du diagnostic sont une thrombocytopénie et une augmentation du temps de céphaline activée (TCA).
La présence de schizocytes sur le frottis est aussi évocateur.
Enfin un profil de coagulation complet montrera souvent :
Ils visent à rétablir l'oxygénation, la microcirculation et à limiter l'agrégation plaquettaire. Donc la fluidothérapie est indispensable avec notamment:
Il est possible d'avoir recours aux ionotropiques pour améliorer la perfusion des organes, notamment des reins.La doputamine s'utilise à la dose de 5-10 mg/Kg/min chez le chien et de 2 à 5 mg/Kg/min chez le chat. Une surveillance de la pression artérielle est nécessaire.
Enfin l'héparine n'est efficace qu'en présence d'anti-thrombine III. Donc l'héparine est en général administrée en même temps qu'une transfusion de sang total et frais prélevé sur citrate. Plusieurs protocoles existent, nous proposons celui-ci:
Elles sont plus rares et se rencontrent notamment lors de mycoses systémiques :
1.2.1. Les hypoplasies mégacaryocytaires.
Elles peuvent être à médiation immune, mais plus souvent elles sont infectieuses ou iatrogènes.
1.2.1.1. Les causes infectieuses.
1.2.1.2. Les causes iatrogènes.
Les médicaments les plus incriminés sont les cytotoxiques utilisés lors des chimiothérapies anti-cancéreuses. Leur pouvoir aplasiant se manifeste souvent, en priorité sur les mégacaryocytes.
Les agents panhypoplasiques se retrouvent également :
De manière plus spécifique on citera :
Elles sont en relation avec une myélodysplasie et se manifestent par la mise en circulation de macrothrombocytes (plaquettes géantes). On les rencontre lors de :
Elle est responsable d'un retard à la formation du clou plaquettaire et de saignements.
2.1.1. Une cause héréditaire : la maladie de Von Willebrand.
Le facteur de Von Willebrand (FVW) augmente la durée de vie du facteur de coagulation VIII et il participe à l'adhésion des plaquettes. La maladie de Von Willebrand correspond à un déficit quantitatif et qualitatif du FVW, elle est surtout présente chez le chien mais très rarement chez le chat.
La maladie se manifeste sur un mode récessif. Les saignements sont principalement muqueux avec une forte prédilection pour l'oro-pharynx et le tractus urinaire. Ils apparaissent souvent avant l'âge d'un an et peuvent être révélés à la faveur d'un traitement AINS. Le diagnostic définitif nécessite le dosage du FVW par des anticorps spécifiques, les réactifs humains n'étant pas adpatés aux carnivores. Le dosage Elisa permet de différencier grossièrement 2 types de la maladie :
Pour information, le type 2 est extrêmement rare chez les animaux et correspond davantage à un déficit qualitatif du FVW, avec des manifestations cliniques sévères.
Les traitements font appel à la transfusion de plasma frais congelé riche en FVW, ainsi qu'à la desmopressine (1 µg/Kg) 1/2 heure avant une intervention à risque (chirurgie, cathétérisme veineux,...)
2.1.2. Les causes infectieuses.
En plus des venins ophidiens certains médicaments sont incriminés.
L'aspirine est un inhibiteur irréversible de la cyclooxygénase-1 (COX-1) contrairement aux autres AINS qui ont une action réversible. De nouvelles générations d'AINS spécifiquement anti-COX-2 n'ont pas d'effet sur la fonction plaquettaire.
Il s'agit des barbituriques et des médicaments utilisés dans le cadre de cardiopathies comme le Diltiazem et le Vérapamil.
2.1.4. Les insuffisances organiques.
L'urémie par inhibition de la fixation du fibrinogène est responsable de saignements. De même pour l'insuffisance hépatique qui conduit à une carence en différents facteurs intervenant dans la formation du clou plaquettaire.
Elle est responsable de la formation de thrombi.
Le syndrome néphrotique, la PIF et la dirofilariose sont sans doute les causes les plus fréquentes. Il semblerait que l'aspirine ne soit pas toujours efficace dans la prévention des thrombi provoqués par les microfilaires.
L'érytropoïetine (EPO) est souvent incriminée.Celle-ci peut être d'origine endogène, notamment lors d'anémies violentes très fortement régénératives, comme les anémies hémolytiques immunes (AHI). Mais elle peut aussi être iatrogène.
Certains carcinomes et sarcomes sont aussi envisagés, mais le mécanisme est totalement inconnu. De plus ces mêmes tumeurs peuvent engendrer une diminution de l'activité plaquettaire.
Enfin le diabète et l'asthme provoquent une hyperactivation plaquettaire chez l'homme, mais rien n'est prouvé chez les carnivores.
Lors de thrombocytose une hyperkaliémie est également à rechercher.
Chien |
Chat |
|
| Normes | <500000 |
<800000 |
| Thrombocytose sévère | >700000 |
>1000000 |
C'est une maladie rare qui se manifeste par une thrombocytose sévère, souvent supérieure à 1000000/mm3. Dans ces conditions les risques de thrombose micro-vasculaire (cerveau, reins, extrémités) sont élevés. De plus, les plaquettes produites sont plus ou moins fonctionnelles, ce qui peut occassionner des saignements.
L'hémogramme révèle une grande variété de forme et de taille des plaquettes, avec la présence de grandes plaquettes hypogranuleuses.
Le myélogramme contient une proportion élevée de mégacaryocytes plus ou moins dysplasiques, mais ils restent inférieurs à 30%. La croissance de ces mégacaryocytes est indépendante de la thrombopoïétine mais le dosage de cette dernière est paradoxalement normal à élevé. Donc sa valeur diagnostique est nulle dans le cadre de la thrombocytémie essentielle.
La thrombocytémie essentielle est indiscernable d'une thrombocytose réactionnelle avec dysplasie que l'on rencontre dans les cas de maladies myeloprolifératives suivantes :
Le diagnostic de la thrombocythémie essentielle est donc un diagnostic d'exclusion. Par ailleurs, la thrombocythémie essentielle ne doit pas être confondue avec la leucémie mégacaryocytaire qui est une leucémie aiguë.
Il n'y a pas de traitement de choix, un protocole de chimiothérapie combinée a semblé être efficace: Cyclophosphamide + Vincristine + Cytosine arabinoside + Prednisone (COAP).
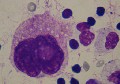 |
Promégacaryocyte : cytoplasme réduit, biploïde avec 2 gros nucléoles. Cette forme blastique est fréquente en cas de LAM7, au niveau du myélogramme. Chat. cliquer sur la photo pour l'agrandir |
Elle est également rare, elle se diagnostique par une quantité de mégacaryocytes supérieure à 30%, au niveau du myélogramme. Souvent, des micromégacaryocytes sont visibles dans la circulation, mais ils sont parfois difficiles à distinguer d'un lymphocyte. Il faudra bien rechercher les excroissances granuleuses neutrophiles ou azurophiles du cytoplasme. Notons encore que ces micromégacaryocytes ne sont pas pathognomoniques et qu'on les rencontre aussi lors de maladies myéloprolifératives. A la différence de la thrombocythémie essentielle, il n'existe pas nécessairement de thrombocytose lors de LAM 7. Une chimiothérapie combinée de type COAP peut être entreprise, mais le pronostic est sombre.
Elles sont en général modérées, elles restent inférieures à 700000/µl. Elles sont d'origines diverses.
Lors d'excitation ou d'exercice physique, il peut y avoir thrombocytose par mobilisation des pools de réserve de la rate et surtout des poumons.
Après une thrombocytopénie sévère il existe une thrombocytose rebond fugace.
Les états hypoxiques liés à des insuffisances cardiaques et/ou respiratoires peuvent occasionner des thrombocytoses graves avec thrombose. Les causes traumatiques, dont les fractures et les chirugies semblent causer plus de thrombocytoses chez les humains que chez les carnivores.
La splénéctomie conduit à une thrombocytose par diminution de la destruction des plaquettes.
Il semblerait que l'interleukine-6 soit le dénominateur commun des thrombocytoses secondaires aux infections, cancers et autres manifestations inflammatoires.
Le Cushing endogène ou iatrogène est responsable de thrombocytose.
La vincristine s'est également révélée thrombocytogène. Son utilisation dans les thombocytoses essentielles peut donc être controversée.